Que a terapia-alvo é o grande ganho no hall de terapias antineoplásicas nos últimos 20 anos, disso ninguém duvida. Ao longo dos últimos anos, drogas como o imatinib (inibidor de BCR-abl tirosina quinase) ampliaram os horizontes de pacientes com Leucemia Mielóide Crônica. Estes, antes da droga, tinham a chance de 1 em 3 de permanecerem vivos após 5 anos e hoje já desfrutam da mesma expectativa de vida de indivíduos sadios após o 2º ano de remissão da doença.[1]
Até então, a terapia-alvo se baseava:
- Em anticorpos específicos contra a neoplasia;
- Em proteínas que, de alguma forma, impediam o crescimento do câncer e levavam a sua morte programada.
Parece bom, não é?
Mas isso não é o bastante! Das bancadas dos laboratórios aos primeiros estudos clínicos, publicados em 2001, as CAR T-cells anti-neoplásicas são a grande reviravolta no contexto do tratamento das Leucemias Linfoblásticas Agudas. [2]
A Leucemia Linfoblástica Aguda (LLA), uma das mais frequentes neoplasias da infância, e apesar de ter menor incidência em adultos, é neste grupo etário que o curso mais dramático. Estimativas inglesas indicam que ao final de 5 anos de LLA, apenas 15% dos pacientes acima de 65 anos estarão vivos. [3] Nas crianças, apesar de a resposta à terapia ser melhor, nos casos de refratariedade ao tratamento, o desfecho também pode ser desanimador. Mas não se abata, as CAR T-cell podem ajudar!
E o que são as CAR T-cells e como elas podem combater a LLA?
- As células T são as grandes maestras da nossa imunidade. Quando bem orientadas, não somente guiam as demais células da imunidade, como atuam por si só contras células tumorais;
- Neste caso, bem orientadas significa restringirem sua atuação de forma ESPECÍFICA à célula que querem atacar, via reconhecimento de antígeno;
- No caso dos cânceres, em especial a Leucemia Linfoblástica Aguda, um grande antígeno se impõe: o CD19. Ele é um “identificador” – cluster domain – das células B, que respondem por mais de 80% dos tipos de células neoplásicas da LLA. Ele também está presente em linfócitos B sadios;
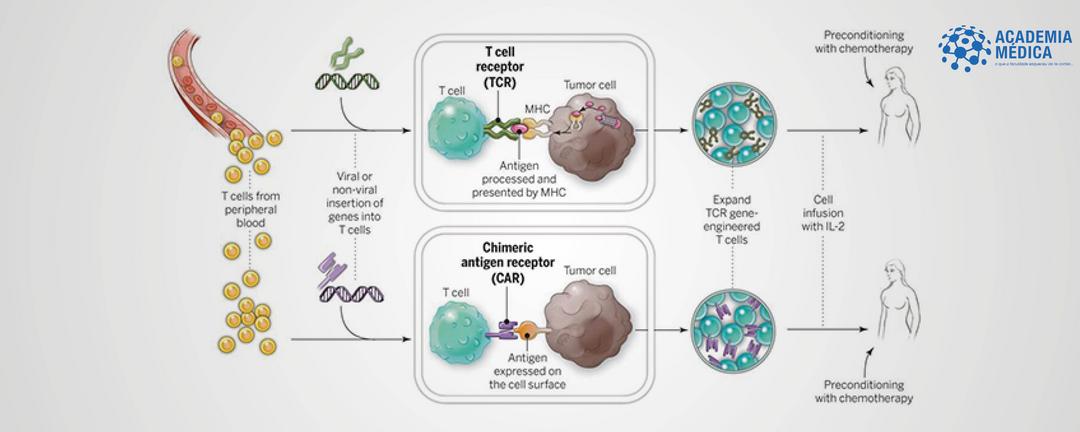
- Sendo assim, a receita para formar uma CAR T-cell é a seguinte: Coleta-se sangue do próprio indivíduo, separando dele a fração de linfócitos T. Nestas células, é feita uma modificação genética, carreada e implantada por vírus, de modo que agora elas são capazes de produzir receptores antigênicos quiméricos (os CAR – chimeric antigen receptors) especificamente contra as células CD19+. Reinseridas no hospedeiro, tais células estão agora programadas para atacar as células leucêmicas! Mais ou menos assim, como mostra o esquema[4]:

- Quando em contato com uma células CD19+, esta CAR T-cell é ativada (inclusive, de forma mais potente que células T normais) e ataca a célula CD19+.
E o que temos de evidências até o momento?
- Estudo publicado em 2014, na New England Journal of Medicine, pelo grupo da Children’s Hospital of Philadelphia and University of Pennsylvania, mostrou a remissão completa da LLA em 27 dos 30 pacientes que receberam as CAR T-cells , mesmo naqueles em que o transplante de células tronco hematopoiéticas havia falhado. E o melhor: estes resultados perduraram pelo menos 24 meses após o início do estudo![5]
- Grupo do Memorial Sloan Kettering Cancer Center (MSKCC) obteve também resultados animadores, com remissão completa em 14 dos 16 adultos (88%) com LLA refratária ao tratamento convencional envolvidos.[6]
Com estes e outros resultados, um grande estudo conduzido pela indústria, agora denominando as CAR T-Cells de tisagenlecleucel (Kymriah™), alavancou a aprovação desta droga pela FDA, que ocorreu em agosto de 2017. Por enquanto, ela é uma opção aceitável ao tratamento de LLA-B refratária em pacientes menores de 25 anos.
Paralelamente ao tratamento da LLA, as CAR-T cell também têm sido testadas para o tratamento de outras neoplasias, como melanoma[7] e mieloma múltiplo, voltadas a antígenos específicos das mesmas.
Ainda é cedo para depositarmos tanta confiança nesta nova modalidade terapêutica aprovada para a LLA. Precisamos de mais estudos que avaliem melhor os efeitos adversos e a longo prazo!
Mas não se preocupe, a ciência está correndo nesse sentido: agora mesmo, em fevereiro de 2018, foi publicado na The New England Journal of Medicine um estudo multicêntrico que contou com um tempo de seguimento médio de 29 meses após o tratamento com a CAR T-cell. Discutirei esse estudo em uma próxima coluna, combinado?
Até breve!
[1] Druker BJ, Talpaz M, Resta DJ, et al. Efficacy and safety of a specific inhibitor of the BCR-ABL tyrosine kinase in chronic myeloid leukemia. N Engl J Med. 2001;344(14):1031-1037
[2] Michael Kalos, Bruce L. Levine, , David L. Porter, Sharyn Katz, Stephan A. Grupp, Adam Bagg, Carl H. Ju. T Cells with Chimeric Antigen Receptors Have Potent Antitumor Effects and Can Establish Memory in Patients with Advanced Leukemia. Science translational medicine. 10 August 2011 Vol 3 Issue 95 95ra73
[3] http://www.cancerresearchuk.org/about-cancer/acute-lymphoblastic-leukaemia-all/survival
[4] Pagel JM, West H. Chimeric Antigen Receptor (CAR) T-Cell Therapy. JAMA Oncol. 2017;3(11):1595.
[5] Maude, Shannon L. et al. “Chimeric Antigen Receptor T Cells for Sustained Remissions in Leukemia.” The New England journal of medicine 371.16 (2014): 1507–1517. PMC. Web. 11 Mar. 2018.
[6] Brentjens, R., Davila, M., Riviere, I., Park, J., Wang, X., Cowell, L. et al. (2013) CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. Sci Transl Med 5: 177ra38
[7] Rosenberg, Steven A. et al. “Durable Complete Responses in Heavily Pretreated Patients with Metastatic Melanoma Using T Cell Transfer Immunotherapy.” Clinical cancer research : an official journal of the American Association for Cancer Research 17.13 (2011): 4550–4557. PMC. Web. 11 Mar. 2018.
Imagem de abertura: CAR T-Cells: Engineering Patients’ Immune Cells to Treat Their Cancers - Nacional Cancer Institute